§ 6. Механизмы акупунктурной анальгезии
Наиболее летально
надсегментарные механизмы, реализующие действие акупунктуры, изучены применительно в анальгезии. Это понятно, учитывая
больше практическое значение данного вопроса и хорошую разработку экспериментальных моделей. В отечественной и зарубежной
литературе существует немало обзоров
и монографических работ, детально анализирующих этот вопрос (БрагинО.Е., 1985; Цибуляк В.Н., 1985; Портнов Ф.Г.,
1987; Решетняк В.Н., 1988; Kendall, 1989; Игнатов Ю.Д. с соавт., 1990 и др"). Поэтому мы, попользовавшись сведениями, изложенными в
этих и других работах, обсудим его достаточно лаконично. Прежде чем обсуждать
механизмы акупунктурного обезболивания, необходимо хотя бы в общих чертах
изложите современную концепцию боли, поскольку и в естественных условиях, и при
различных методах обезболивания болевая
(ноцицептивная) и противоболевая (антиноцицептивная) системы находятся в постоянном взаимодействии,
В настоящее время большинством авторов принято мнение о существовании
специфи-ческих болевых
рецепторов (ноцндепторЪв), реагирующих на какую-либо
модальность (давления, температуру и т.д.),
оказывающую разрушительное воздействие на ткани, или на множество типов
воздействий полимодальные ноцицспторы).
Эти ноцицепторы связаны с нервными
афферентами 2 типов - А-дельта и С. Моно, бимодальные ноцицеп-торы проводят импульсацию по А-дел-ьта
волокнам, а большинство полимодальных - по С волокнам. Как известно, на основании характера воспринимаемого
болевого ощущения, боль разделяют на 2 вида - эпикри-тическую и
протопатическую. Первая из них характеризуется практически мгновенным
восприятием, точной локализацией и опознаванием характера повреждающего
воздействия. Вторая - имеет больший латентный период, менее четко позволяет дифференцировать
место и качество вредоносного агента, сопровождается значительной эмоциональной реакцией. К первому виду боли наблюдается
привыкание (устранение болевого ощущения
при повторных многократных воздействиях), второй при этом только усиливается.
Выяснено, что эпикритичсская боль
воспринимается и проводится А-дельта афферентами с достаточно высокой скоростью
проведения импульсов 4-40 м/с, протопатическая - С-афферентами - со
скоростью проведения 0,4-2 м/с. Хемоноцицспторы,
реагирующие на изменение химизма тканей, и, главным образом, на уровень
кислородного обеспечения, относят к
С-ноцицепторам, являющимся рецепторами и проводниками патологических воздействий
на ткани внутренних органов, сосудов, кожи, нервов.
Ноцицепторные афференты, приходя в задние рога спинного
мозга, распрострайяются в желатинозной субстанции.
В I пластину по Рекседу в основном
приходят А-дельта болевые волокна, во II - тонкие
С-ноци-цептивные и неноцицептивные волокна. Ноцицептивные и неноцицептивные
волокна распространяются и в более глубоких слоях желатинозной субстанции. По мнению
Ю.Д.Игнатова и соавт. (1990), основную роль в распознавании вредоносности
воздействия выполняют клетки V слоя, на которые
конвергируют ноцицептив-
ныс и неноцицептивные кожные и висцеральные
афференты. Последняя оказывает модулирующее воздействие на проведение импульсов из периферических
волокон на клетки (Melzack R., Wall P., 1982). При этом происходит взаимное влияние разных волокон с торможением проведения
импульсации одними в других. Так, клетки
желатинозной субстанции, возбуждающиеся болевой импульсацией, тормозятся при
неноцицептивной стимуляции, а
клетки, тормозящиеся ноцицептивной импульсацией, активизируются при
неноцицептивном раздражении (Решетняк В.К., 1985). Этот механизм лежит в
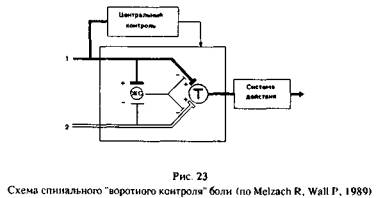
основе концепции воротного контроля боли Мслзака и Уолла (1965). Согласно этой
концепции (рис.23), афферентная импульсация, приходящая по толстым
быстропроводящим волокнам, активизирует нейроны первого-центрального
переключения T.
(transmission) нейроны.
Одновременно через коллатерали эта импульсация возбуждает нейроны в желатиноз-ной субстанции,
которые, вызывая пресинаптическое торможение, затрудняют проведение импульсов
по обоим
видам волокон. При болевом воздействии достаточной надпороговой интенсивности
активизированные тонкие А-дельта и С-волокна тормозят Т-нейроны и снимают торможение в
афферентах, открывая таким образом "ворота" для афферентной ноцицептивной
импульсации. Т-нейроны через восходящие пути активизируют структуры головного
мозга, вызывая целостную болевую реакцию. Аналогичные механизмы регулирования проведения
болевой импульсации действуют на других уровнях. Спинальный уровень контроля
входа боли
находится под регулирующим влиянием надсегментарных структур мозга. Наиболее
вероятным местом функционирования контрольного механизма является I и II слои желатинозной
субстанции, получающие терминали аксонов от многих толстых и тонких волокон и
дендриты клеток из более глубоких слоев. Это образование прослеживается на всем
протяжении спинного мозга, соединяясь в его оральных отделах с аналогичной
структурой тригеминальной системы (MelzackR., 1986).
Болевая чувствительность в головной
мозг проводится по трем основным путям - спиноталамическому, спиноретикулярному и
спиномезенцефальному, объединеннным в передний спинномозговой тракт. Он разделяется на
неоспиноталамический путь и палеоспиноталамический путь, объединяющий
спиноретикулярный и спиномезенцефальный пути.
Кроме этого, ноцицептивная афферентация
распространяется по спиноцервикальному тракту, оканчивающемуся в латеральном
шейном ядре, по тракту Лиссауэра, задне-боковому проприоспинальному и дорсальному интракорнуальному
тракту.
Наиболее важным
трактом, по которому проводится первичная, эпикритическаяболь, является
олитосинап-тический неоспиноталамический, в который посылают волокна
специфические ноцицептивные нейроны желатинозной субстанции. Скорость проведения по
этому пути составляет 47-60 м/с (Taira et al, 1984).
Основная часть волокон
неоспиноталамического тракта заканчивается в заднем вентролатеральном ядре зрительного бугра.
Болевая афферентация с лица и слизистой ротовой полости поступает в каудальное
ядро тройничного
нерва, морфофункциональные характеристики которого аналогичны задним рогам
спинного мозга.
Далее афферентация отсюда также приходит в зрительные бугры - в основном в
заднее вентромедиаль-ное ядро. Таким образом, аксоны специфических
ноцицептивных нейронов приходят в вентробазальный комплекс зрительных
бугров, являющийся релейным образованием, проводящим сенсорно-дискрйминатив-ные ощущения
поверхностной чувствительности. Из вентрюбазального комплекса зрительных бугров
афферентация далее поступает
в основном в область С2 теменной коры, где обнаружено большее число соматотопически организованных специфических
ноцицептивных нейронов (Решетняк В.Н., 1985). Вся описанная система и обеспечивает быстрое и точное
определение локализации и характера повреждающего воздействия.
Вторичная прогопатическая
боль распространяется по аксонам нейронов из более глубоких пластин жеала-тинозной субстанции,
объединенных в мультисинаптический медленно проводящий палеоспиноталамический тракт. Он приходит к
ядрам ретикулярной формации каудального и рострального отделов ствола мозга, медиальным и
интраламинарным ядрам зрительных бугров, откуда далее диффузно распространяется
в кору мозга,
лимбическую систему, гипоталамус и базальные ганглии. Таким образом,
обеспечивается эмоциональный, поведенческий и вегетативно-эндокринный компонент
болевой реакции.
Весьма не просто
выглядит нейрохимическое обеспечение ноцицепции. Многочисленные исследования в этой области часто
противоречивы, что понятно, учитывая сложность вопроса - см. обзоры
В.К.Решетняка (1981) и Е.О.Брагина (1985). В клетках ганглиев задних корешков
обнаружены субстанции P, ангиотензин II и соматостатин.
Волокна их в основном связаны с нейронами I
и II слоя желатинозной субстанции. Кроме этого, часть клеток ганглия
содержит моноамины и динорфин. Обнаружена также возможность выделения субстанции
P в свободных нервных окончаниях при антидромном проведении возбуждения. В
задних рогах спинного мозга и каудальном ядре тройничного нерва, помимо
приносимых афферентами клеток дорсального спинномозгового ганглия субстанции P,
ангиотензина II и соматостатина, обнаружены
нейротензин, энкефалин и динорфин. Во всех слоях желатинозной субстанции выявлены
нервные терминали нисходящих трактов, направляющихся из бульварного ядра шва, несущие
серогонии и норадреналин. Энкефалин и нейротензин вероятно участвуют в качестве
передатчиков или модуляторов в интернейронах задних рогов. Эти и другие нейропептиды и
моноамины обнаруживаются в различных структурах головного мозга, и в наибольших
концентрациях
- в основных ноцицептивных структурах - ядрах шва, околоводопроводном сером
веществе и миндалине, а также в зрительных буграх, базальных ганглиях,
гипоталамусе, гипофизе и лимбической системе (Rullingham, 1985).
Перечисленные и другие нейрохимические
агенты обеспечивают функционирование ноцицептивной и антиноцицептивной
систем мозга. Последняя включает в себя ядра шва ствола мозга, центральное
серое вещество,
парагигантоклеточное ядро ретикулярной формации, хвостатое ядро, таламус,
гипоталамус, красное ядро, черную субстанцию, мозжечок, кору больших полушарий. Одними из
главных ключевых образований в антиноцицептивной системе мозга являются
центральное серое вещество и ядра шва. При стимуляции ядер шва повышается
порог болевой реакции и подавляется проведение ноцицептивной импульсации в спинном мозге, ядрах
тройничного нерва и в вышележащих структурах головного мозга (Решетняк В.И.,
1985). Этот
процесс обеспечивается серотонинсодержащими и норадреналиэргическими нейронами,
отростки которых распространяются в нисходящем направлении по дорзолатеральному
тракту к нейронам желатинозной субстанции спинного мозга и в межуточный мозг. Последний
связан с лимбической системой, принимающей участие в регуляции эмоциональных и
поведенческих компонентов болевой реакции. Стимуляция центрального серого вещества
вызывает у экспериментальных животных еще более сильный анальгегический эффект,
который
опосредуется различными нейрохимическими агентами. Раздражение голубого пятна,
главного но-радренэргического ядра мозга, также, по данным Hodge et al (1983), продуцирует анальгетический эффект, хотя существуют и
другие сведения о тормозном влиянии этого образования на акупунктурную
анальгезию (см. Игнатов Ю.Д. и соавт., 1990).
Антиноцицептивный
эффект стимуляции структур нигрокаудатной системы, по-видимому, может реализоваться за счет
тормозных влияний на ядра зрительного бугра и связей с ядрами шва. Существенное
значение в функционировании антиноцицептивной системы имеет гипоталамус и
главным образом его аркуатное ядро, в котором, как полагают, происходит синтез
нейропептидов, транспортируемых оттуда в гипофиз. Кроме этого, гипоталамус
может влиять на проведение и перцепцию боли через прямые связи со спинным
мозгом и корой головного мозга, Роль таламуса в торможении проведения боли,
показанная в эксперименте и клинике, осуществляется путем задействования его
связей с ядерными образованиями ствола мозга. На уровне коры мозга происходит
модуляция деятельности подкорковых ангиноцицептивных структур, при этом, по
данным В.Н.Решетняка
(1985), наибольшее значение имеет С2 область сенсорной коры. Кромеэтого, важное
значение ямеют
проекции из лобной коры, через которые осуществляются регулирующие влияния
когнитивных процессов (память, внимание). Это обеспечивается через корковую
ретикулярные связи и пирамидный путь, частично проецирующийся и в задние рога.
Этим обеспечивается участие коры в общем механизме контроля боли,
Как показывают экспериментальные
данные и клинические наблюдения, акупунктурное обезболивание оказывает наиболее
полный эффект, подавляя не только субъективное восприятие боли, но и
сопровождающие ее эмоционально-аффективные и вегетативные компоненты (Игнатов Ю.Д. и
соавт., 1990).
Применение иглотерапии для анальгезии
является одним из древних народных способов обезболивания, в основе которых лежит
рефлекторный принцип - прижигание, охлаждение, наложение раздражающих веществ,
электровоздействие (использования электропродуцирующих рыб-скатов); апитерапия
и т.д. Мелзак эти методы обезболивания называет гиперстимуляционной анальгезией. В
настоящее время более распространенным методом анальгезии в экспериментальных
и клинических целях является электропунктура, позволяющая тонко дозировать
интенсивность и другие параметры воздействия, что позволяет при необходимости "включать"
различные виды рецепторов. близким к
электропунктуре методом является чрезкожная электро-нейросгимул яция,
лазеропунктура.
Одним из механизмов реализации
акупунктурной анальгезии на сегментарном уровне, по-видимому, является торможение
ответов нейронов V слоя задних рогов спинного мозга и
каудального ядра тройничного нерва на болевое раздражение (Игнатов Ю.Д. и
соавт., 1990). Медленное развитие анальгезии в течение 10-20 мин. свидетельствует о
вероятном включении гуморальных механизмов, а именно - выделении эндорфинов и энкефалинов,
оказывающих тормозное воздействие на проведение болевой импульсации.
Предполагается, что акупунктурное воздействие через толстые нервные волокна
(объединяющие, в частности, мышечные аффе-ренты) осуществляет "включение"
нейронов желатинозной субстанции, и, как следствие, развитие пресинап-тического
торможения, закрывающего "ворота" дла болевой импульсации. Из
практики известно, что наиболее эффективно анальгезию можно вызвать,
стимулируя точки акупунктуры, локализующиеся над мышечными массивами. Интересно
и соответствие между триггерными болевыми зонами при миофасциальных синдромах и локализацией точек
акупунктуры. Специальный анализ показал, что все описанные тригтерные зоны находятся в области
точек акупунктуры, хотя, конечно, число последних значительно больше (Melzack R., 1977), Существует точка зрения и о том, что
ненецицептивные раздражения в зоне иннервации, находящейся вне сегментов, куда
проецируется основная болевая афферентация, может угнетать ноцицептивные
нейроны Y
слоя. Это подтверждается клиническими и эксперминтальными данными о том, что
наибольший анальгетический эффект достигается при задействовании наряду с
толстыми А-бета волокнами и тонких А-дельта волокон (Решетник В.Н., 1985).
В реализации акупунктурного
обезболивания важнейшее участие принимают надсегментарные церебральные структуры.
Прежде всего запуск и контроль функционирования антиноцицептивной системы
осуществляется
болевой лемнисковой спиноталамической системой. При ее экспериментальном
повреждении или патологическом изменении в условиях соответствующих неврологических
заболеваний не происходит адекватного функционирования антиноцицептивной системы
("таламическая боль"). Акупунктурная анальгезия осуществляется при
активации по существу всех церебральных структур, входящих в антиноцицептивную систему -
гигантоклсточного ядра ретикулярной формации, связанного с центромедиальным
ядром таламуса, ядра шва, центрального серого вещества, аркуатного ядра гимоталамуса,
хвостатого ядра, септальной области. Возбуждение нейронов в этих структурах при
акупунктурном воздействии вызывает торможение восприятия и проведения болевой
импульсации в спинном мозге, релейных ядрах таламуса, тормозит ноцицептивные клетки соматосенсорной
коры. Одновременно устраняются и вегетативно-эндокринные проявления болевой реакции, вследствие
блокирования реагирования со стороны гипоталамуса и лимбической системы.
Разрушение структур
антиноцицептивной системы в эксперименте в разной мере уменьшает или даже устраняет эффект
акупунктурного или электропунктурного обезболивания.
Ключевыми
структурами, активация которых необходима для достижения обезболивания,
являются центральное серое вещество и ядра шва, на которые проецируются влияния многих
других церебральных ядерных образований. Сложность, гетерогенность антиноцицептивной
системы, по мнению В.Н.Решетняка, обусловливает необходимость применения двух
различных частот электропунктурной стимуляции - в диапазоне 1-3 гц, когда возникает субболевое
возбуждение А-дельта волокон, проецирующееся в центральное серое вещество
77
и более высокой - 10 гц. Различные параметры стимуляции вызывают и
разные нейрохимические процессы, лежащие в основе обезболивания (Е.О.Брагин,
1985).
Среди химических посредников
обезболивания в последнее время наибольшее внимание уделяется нейро-пептидам и
моноамикам. Косвенными признаками участия гуморальных факторов в акупунктурном
обезболивании, как уже говорилось, является постепенное развитие эффекта и его
сохранение какое-то время после окончания воздействия, возможность снижения
эффекта при длительном и частом применении этого метода. Среди нейропептидов
наибольшее значение в реализации анальгетического эффекта придается эндорфинам.
энкефалину, динорфину, действующим на разных этажах нервной оси. Эндорфины
(вероятно, бетаэндорфин) функционируют на уровне ствола мозга
(околоводопроводное серое вещество, ядра шва). зрительных бугров, сегментарного
аппарата спинного мозга. Источником эндорфинов, как предполагается, является
гипофиз, при экспериментальном устранении которого анальгетический эффект
значительно ослабевает. Выделяющийся из гипофиза бегазндорфин, синтезируемый в
аркуатном ядре гипоталамуса, затем различными путями транспортируется во многие отделы
антиноцицептивной системы, включая задние рога спинного мозга, где он тормозит активность релейных Т-нейронов, закрывая
"входные ворота" боли (Игнатов Ю.Д. и соавт., 1990). Участие эндогенных морфиноподобных веществ в
акупунктурной анальгезии подтверждается и уменьшением или полным устранением
эффекта стимуляции после введения налоксона - антагониста опиатных рецепторов.
На сегментарном уровне большое значение имеют две других
группы нейропептидов - энкефалины и динорфин,
которые, как уже говорилось, в большом количестве выделены в желатинозной
субстанции задних рогов спинного
мозга. Здесь же высока плотность и динорфиновых рецепторов. Введение в
субарахноидальное пространство спинного мозга антиэнкефалиновой и
антидинорфиновой сывороток значительно снижало у экспериментальных животных анальгетический эффект акупунктуры (Нап,
1984). Существуют данные о том, что выделение энкефалина происходит при
электропунктурной стимуляции с низкой частотой (8 гц), а динорфина - при высокочастотной стимуляции (100
гц). При этом предполагается, что низкочастотная стимуляция активирует А-дельта волокна, а
высокочастотная - С-афференты (Wangetal 1985; Pel et al 1985).
Эффект развития
толерантности к акупунктурной анальгезии, объяснявшийся ранее истощением
эндогенных опиоидных пептидов, в последнее время связывается с действием
холецисгокинина. Он присутствует в обычных условиях в небольших количествах и оказывает умеренное
тормозное воздействие на активность опиатэргической системы. При активации
последней увеличивается и выброс холицистокинина. Введение антисыворотки к этому веществу замедляет развитие
толерантности к акупунктурной анальгезии.
Возможно, что
развитие толерантности обусловлено и действием ангиотензина II (Нап, 1988), также выделенного в задних рогах спинного мозга.
Важнейшую роль в регуляции болевой чувствительности играет
серотонин, значение которого в этом процессе
понятно уже довольно давно. В наибольшей концентрации он находится в
околоводопроводном сером веществе и ядрах шва - ключевых структурах
антиноцицептивной системы, впрочем не только ее. Аксоны серотонинэргических нейронов отсюда распространяются по всем основным
подкорковым структурам, в лим-бическую систему, кору, а также к задним
рогам спинного мозга и дорзальному ядру тройничного нерва, регулируя таким образом различные функциональные
системы и аспекты поведения животных и человека. Воздействия, приводящие к
снижению концентрации серотонина (торможение синтеза, усиление распада),
разрушающие указанные ядра, блокада серотониновых рецепторов, снижают
анальгетический эффект фар-макопрепаратов, в том числе опиатов и акупунктуры.
Напротив, акупунктура способна вызвать повышение уровня серотонина в плазме и тромбоцитах. Фармакопрепараты, усиливающие
действие этого нейромедиато-ра,
увеличивают и эффект акупунктурной анальгезии (Игнатов Ю.Д. и соавт., 1990).
Действие серогонинэргической системы
функционально связано с опиодной системой, в частности, с бета-эндорфинами на
уровне головного мозга и с энкефалинами - на спинальном сегментарном уровне.
Наряду с серотонинэргической системой,
в обеспечении анальгетического эффекта участвуют и норадрена-лин. Основное ядро
ствола мозга, где он находится в наибольшей концентрации - голубое пятно. Также
как и ядра
шва, это полифункциональное образование оказывает диффузное воздействие на
различные функции мозга путем распространения медиатора по аксонам во многие структуры
головного мозга (ствол, гипоталамус, таламус, лимбическая система, кора) и в
задние рога спинного мозга. В отличие от серотониновой системы катехоламины
оказывают тормозящее действие на акупунктурную анальгезию, что доказывается
усилием анальгетического
эффекта после разрушения голубого пятна или снижения уровня норадреналина в
этой системе.
Этот эффект достигается торможением активности серотонинэргических нейронов
ядер шва. Существуют данные и о том, что норадренэргическая медиаторная
система может оказывать положительное влияние на реализацию акупунктурнога
обезболивания на уровне сегментарных структур спинного мозга. Таким образом, эффект
зависит от того, на каком уровне включается эта медиаторная система.
Положительное действие на акупунктурную анальгезию оказывает и дофамин, обеспечивая
вместе с серотонином нисходящее из ядер ствола мозга торможение ноцицептивных
спинальных нейронов (Игнатов Ю.Д. и соавт., 1980). Участие
холинэргических и гамкэргических систем в реализации эффекта акупунктурной
анальгезии менее определенно.
Возвращаясь к концепции контроля
входа боли, наиболее адекватно суммирующей механизм акупунктурной анальгезии,
приведем точку зрения на этот счет одного из ведущих специалистов по проблеме
боли Ронолда Мелзака (MelzackR, 1986).
Мелзак отмечает 3 главных качества
гиперсгимуляционной, в том числе акупунктурной, анальгезии: 1) необходимость
воздействия средними или интенсивными по силе раздражениями; 2) раздражение
может быть
нанесено в зоне, далекой от источника боли; 3) достаточно
кратковременное воздействие может устранять боль на длительное время.
По мнению автора этой концепции, центральным звеном системы
является ствол мозга, оказывающий мощный тормозной контроль над проведением
боли. Эта область получает афферентацию от всех структур тела и широко распространяет свои влияния по
головному и спинному мозгу. Стимуляция поверхности тела акупунктурой или другими способами, вызывающая
активацию тонких волокон, продуцирует дополнительный приток в
центральный контролирующий механизм, который может закрыть вход афферентации из
соответствующих частей тела. Поскольку известна соматотопическая организация
ретикулярной формации ствола мозга, то можно полагать, что определенные части
тела проецируются в соответствующие участки ретикулярной
формации, которые, в свою очередь, закрывают вход для патологической болевой
афферентации на соответствующих
уровнях спинного мозга или ствола.
Пролонгированный эффект обезболивания
предполагает наличие реверберационной активности в этих нейронных системах, поддерживаемый умеренной афферентацией из
патологического очага и физиологической
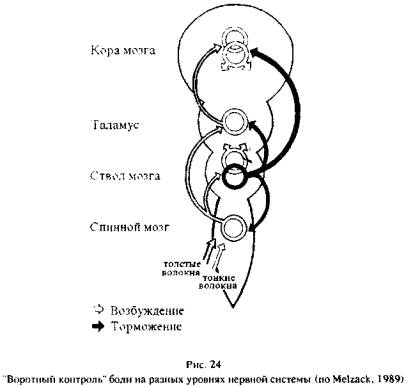
афферентацией, усиливающейся на фоне снятия боли. Эта концепция в схематическом
виде приведена на рис. 24. Видно, что
толстые и тонкие волокна активируют нейронные комплексы в спинном мозге, которые,
в свою очередь, оказывают
возбуждающее влияние на надсегментарные структуры. Центральным контролирующим механизмом является ретикулярная формация
ствола мозга, оказывающая модулирующее воздействие на структуры головного мозга и спинной мозг. Близкой к этой
концепции является гипотеза Босси (Bossy ;.,
1973), о роли ретикулярной формации в обеспечении эффекта акупунктуры, в том
числе анальгезии, юдробно приведенная в
монографии Ф.Г.Портнова (1987).
В этой схеме на наш взгляд
недостаточно подчеркивается сегментарный компонент акупунктурной анальгезии,
который, как известно из практики, наряду с точками общего воздействия,
стимуляция которых скорее всего обращена к надсегментарным стволовым структурам,
имеет существенное значение для местного обезболивания.
Следует заметить, что описанные
нейрофизиологические и нейрохимические механизмы, обеспечивающие акупунктурную
анальгезию, столь же большое значение имеют и в реализации других эффектов
акупунктуры, поскольку в регуляции висцеральных, нейроэндокринных функций,
мотиваций, эмоционального состояния, сна и бодрствования, внимания эти
церебральные структуры и медиаторные системы играют ключевую роль. Именно этим
и объясняется общеорганизменное, адаптогенное действие акупунктуры и ее
аналогов.
Так, за счет активации эндорфинов, акупунктура может
оказывать положительное действие при таких состояниях как депрессия,
алкоголизм, наркомания, нарушения сна, алиментарное ожирение, артериальная гипертония и др.

Сайт управляется системой
uCoz
